Организм умеет уничтожать патогены, с которыми сталкивался ранее. Эта способность называется приобретенным иммунитетом. Приобретенный иммунитет может убивать инфицированные вирусом клетки и генерировать защитную иммунологическую память. Именно она является основой стратегий вакцинации.
Для борьбы с вирусами и развития иммунологической памяти важны ответы Т-клеток и В-клеток. Попадая в клетку организма, вирусы берут на себя управление клеточными механизмами, чтобы создавать новые вирусные частицы и распространяться на здоровые клетки. Вирусные инфекции вызывают врожденные иммунные реакции, например, воспаление. Эти реакции активируют приобретенный иммунитет. Дендритные клетки захватывают вирусные белки и частицы и транспортируют их в лимфоидные органы – селезенку и лимфатические узлы. Там вирусные белки и частицы распознаются Т- и В-клетками. Клеточная (Т-клеточная) и гуморальная (В-клеточная) ветви приобретенного иммунитета работают вместе, обеспечивая вирус-специфическую защиту.
Механизм распознавания и устранения вируса
Как Т-клеточное распознавание вирусных пептидов, так и В-клеточное распознавание вирусных белков начинаются в лимфоидных тканях, где дендритные клетки представляют пептиды Т-клеткам, а В-клетки отбирают вирусные белки. Вместе они инициируют развитие эффекторных клеток для устранения вируса.
Величина ответов Т- и В-клеток определяется:
- патогенностью вируса;
- степенью воспаления;
- частотой вирус-специфических Т- и В-клеток;
- кинетикой репликации вируса.
CD8+ Т-клетки – T-киллеры – дифференцируются в эффекторные клетки, которые ограничивают репликацию вируса, уничтожая инфицированные клетки. CD4+ Т-клетки – T-хелперы – дифференцируются в эффекторные клетки, которые подавляют репликацию вируса и поддерживают CD8+ Т-клетки, а также дифференцировку В-клеток. Как CD8+, так и CD4+ Т-клетки продуцируют противовирусный и иммуномодулирующий пептид интерферон гамма. Чтобы запустить противовирусную реакцию, эффекторные Т-клетки могут проникать в кровоток и перемещаться к очагам инфекции.
CD4+ Т-клетки также дифференцируются в фолликулярные Т-хелперы (ТFH), которые необходимы для развития продуцирующих антитела В-клеток и поддерживают развитие В-клеток памяти. ТFH имеют решающее значение для формирования зародышевых центров в фолликулах периферических лимфоидных органов.
Антитела могут нейтрализовать вирусы, предотвращая проникновение в клетки или способствуя гибели инфицированных клеток. В результате скоординированного взаимодействия врожденного и приобретенного иммунитета пиковые реакции Т- и В-клеток приводят к снижению вирусной нагрузки и ослаблению воспаления, часто в течение одной недели после заражения.
T- и B-клетки памяти
После удаления вируса большинство эффекторных Т- и В-клеток погибают. Сохранившиеся Т-клетки становятся Т-клетками памяти. Сохранившиеся В-клетки генерируют либо долгоживущие плазматические клетки, продуцирующие антитела, либо становятся В-клетками памяти. Клетки памяти способны быстро реагировать на повторное заражение.
SARS-CoV-2-специфические CD4+ и CD8+ Т-клетки обнаруживаются в кровотоке как у активно инфицированных, так и у выздоровевших пациентов, что свидетельствует о потенциальной способности развития защитного клеточного иммунитета.
Т-клетки памяти бывают:
- эффекторными – реагирующими при высоких титрах вируса;
- центральными – служащими резервуаром для защиты во время будущих реинфекций.
Т-клетки, расположенные в очагах инфекции, могут стать тканево-резидентными T-клетками памяти (TRM).
Что определяет эффективность приобретенного иммунного ответа
Когда приобретенные иммунные ответы на инфекцию неоптимальны или вирус развил средства для уклонения от иммунных ответов (включая подавление вирусом иммунитета), может наступить хроническая инфекция или системное заболевание и смерть, особенно у лиц из группы риска. Тяжесть заболевания при коронавирусе SARS-CoV-2 различна. Поэтому необходимо понимать, какие факторы определяют эффективность приобретенного иммунного ответа и длительный защитный иммунитет, особенно в уязвимых группах населения: пожилых и людей с ослабленным иммунитетом.
Ключевой фактор в устранении вирусных инфекций – устойчивые высокоэффективные противовирусные реакции Т- и В-клеток. Наивные Т- и В-клетки имеют на поверхности разнообразные рецепторы вирусного распознавания, поэтому могут распознавать широкий диапазон вирусов. Во время инфекции отбираются T-клетки с наиболее подходящими T-клеточными рецепторами – они обладают большей способностью связывать вирусные пептиды. Сродство B-клеточных рецепторов к вирусным белкам продолжает увеличиваться в ходе инфекции через процессы соматической гипермутации и клональной экспансии. Соматическая гипермутация – механизм, обеспечивающий разнообразие B-клеточных рецепторов и антител. Благодаря ему иммунная система может распознавать больше различных патогенов. Клональная экспансия – процесс деления B-клеток, при котором из одной клетки появляется множество копий.
B-клетки переключаются с раннего синтеза антител класса M (IgM) на синтез антител IgG и IgA с более высоким сродством. Эти антитела обнаруживаются в сыворотке выздоравливающих пациентов с COVID-19.
Величина ранних ответов антител может свидетельствовать о тяжести инфекции, поскольку более высокие титры антител IgM и IgG ассоциированы с более тяжелым заболеванием. Как и в случае с другими вирусными инфекциями, общие титры антител к SARS-CoV-2 в сыворотке крови уменьшаются после излечения активной инфекции. Однако долгоживущие В-клетки памяти могут сохраняться и продуцировать циркулирующие вируснейтрализующие антитела. Недавнее исследование показало, что через 6-8 месяцев после начала заболевания COVID-19 нейтрализующие антитела против SARS-CoV-2 были обнаружены у 90% выздоровевших пациентов. Также важно отслеживать и сравнивать продолжительность реакции В-клеток памяти на естественную инфекцию SARS-CoV-2 и вакцины.
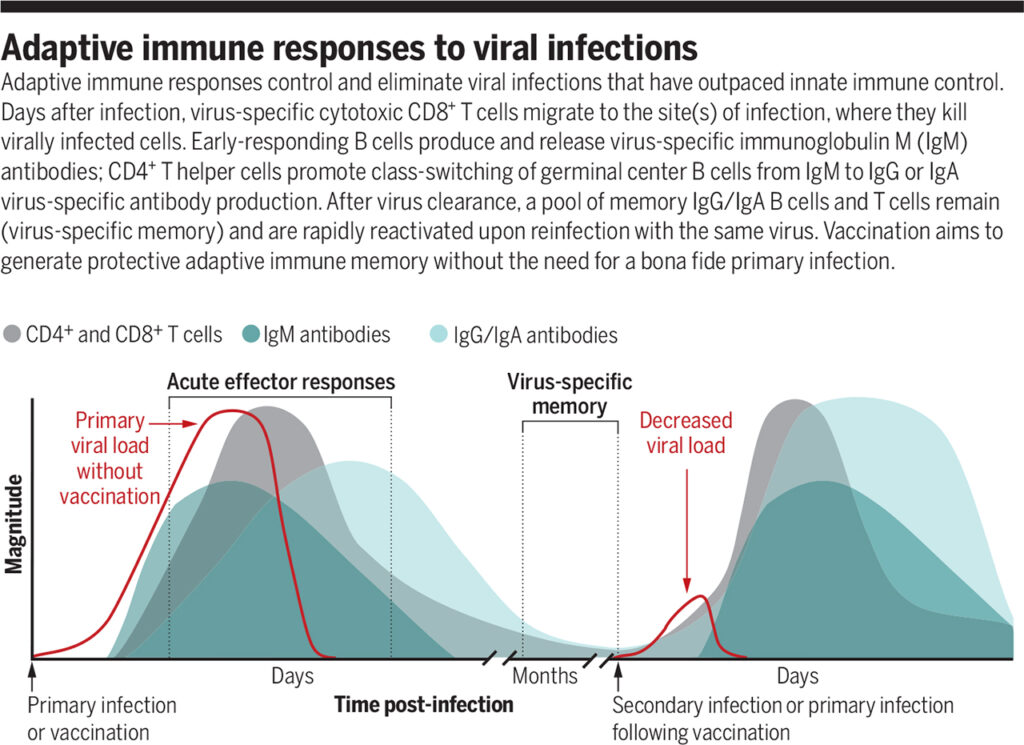
Приобретенный иммунный ответ на вирусные инфекции
Источник: https://www.science.org/doi/full/10.1126/science.abf6446
Приобретенный иммунный ответ контролирует и устраняет вирусные инфекции, опередившие врожденный иммунный контроль. Через несколько дней после заражения вирус-специфические цитотоксические CD8+ Т-клетки мигрируют к месту инфекции, где убивают инфицированные вирусом клетки. В-клетки с ранним ответом продуцируют вирус-специфические антитела IgM. CD4+ Т-хелперные клетки способствуют переключению класса В-клеток зародышевого центра с IgM на IgG или выработке вирус-специфических антител IgA. После удаления вируса сохраняются B-клетки памяти IgG / IgA и Т-клетки памяти. Они быстро реактивируется при повторном заражении тем же вирусом. Вакцинация направлена на формирование защитной приобретенной иммунной памяти без необходимости в подлинной первичной инфекции.
Перекрестно-реактивные T- клетки и антитела
На ответы приобретенного иммунитета могут влиять предыдущие встречи с вирусами. Например, ТRM-клетки, находящиеся в легких, могут распознавать внутренние структурные белки вирусов гриппа и впоследствии снижать тяжесть заражения новыми штаммами вируса гриппа. Т-клетки, реактивные к белкам SARS-CoV-2, были обнаружены у лиц, ранее инфицированных SARS-CoV, и у здоровых людей, не подвергавшихся воздействию этих коронавирусов. Эти результаты показывают, что Т-клетки памяти генерируются при заражении другими коронавирусами человека (HCoV), включая простудные коронавирусы. Было обнаружено, что антитела IgG пациентов с COVID-19 сильно реагируют на белки вируса гепатита C. Напротив, SARS-CoV-2-реактивные антитела, специфические для белков HCoV, были обнаружены в сыворотках людей, не болевших COVID-19, – это могут быть широко нейтрализующие антитела.
Пока неясно, могут ли уже существующие SARS-CoV-2-реактивные Т- и В-клетки способствовать улучшению исходов заболевания. Если они улучшают исход заболевания, то может быть желательно увеличить такие популяции Т- и В-клеток с помощью вакцинации.
Чем опасна чрезмерная активация T-клеток
Важно отслеживать степень инфицирования и воспаления, вызванного вирусами, включая SARS-CoV-2. Чрезмерные врожденные иммунные ответы, такие как гипервоспаление (повышенный уровень интерлейкина-6 (IL-6) и С-реактивного белка), могут способствовать выраженной активации Т-лимфоцитов, которая еще больше усиливает воспаление и тяжесть заболевания. Обширная активация Т-клеток во время COVID-19 может привести к лимфопении (уменьшению количества лимфоцитов), изменению дифференцировки и потере функции Т-клеток. Это может замедлить вирусный клиренс, продлить инфекцию и повысить заболеваемость.
Факторы, прогнозирующие тяжесть заболевания
Остается неясным, почему у некоторых инфицированных людей симптомы отсутствуют, тогда как у других наблюдается тяжелый COVID-19. Однако с тяжелым COVID-19 связаны:
- Нарушение врожденных иммунных ответов интерферона I типа.
- Цитомегаловирус (CMV) и вирус простого герпеса 1 (HSV-1).
- Мужской пол. Мужчины, госпитализированные с COVID-19, имеют более сильный ответ антител и повышенную тяжесть заболевания по сравнению с женщинами.
- Возраст > 65 лет. У пожилых людей во время острой инфекции SARS-CoV-2 чаще наблюдались нерегулируемые реакции приобретенного иммунитета, чем у более молодых людей.
- Ранний профиль антител. Американские ученые обнаружили, что ранние различия в профилях антител к спайковому белку (S) и белку нуклеокапсида (N) коронавируса SARS-CoV-2 прогнозируют легкое или тяжелое течение COVID-19. S-антитела были повышены у выздоравливающих людей, тогда как N-антитела были повышены у умерших пациентов. Напротив, устойчивые Т-клеточные ответы на S, N и мембранный белок (M) не были связаны с лучшим выздоровлением у критически больных пациентов с COVID-19.
- Состав кишечного микробиома. Американские исследователи показали, что увеличение количества кишечных бактерий Enterococcus faecalis – главный предиктор тяжелого COVID-19.
Возможность выявления прогностических факторов будет увеличена за счет включения бессимптомных лиц, инфицированных SARS-CoV-2.
Опасные реакции приобретенного иммунитета на коронавирус SARS-CoV-2
Немецкие ученые обнаружили, что у активно инфицированных пациентов сильно мутировавшие рецепторы B-клеток и снижение клональной экспансии были связаны с более тяжелыми клиническими исходами, тогда как больший пул вирус-специфичных наивных В-клеток у пациентов коррелировал с развитием более эффективного противовирусного иммунного ответа.
Усиленная дифференцировка TH1, потеря TFH и связанное с этим отсутствие формирования зародышевого центра были недавно обнаружены при посмертном анализе лимфатических узлов и селезенки у пациентов, которые скончались в течение 10 дней с момента появления респираторных симптомов COVID-19. Измененные пропорции субпопуляций CD4+ Т-клеток периферической крови, статуса активации Т-лимфоцитов CD8+ и В-клеток также наблюдались у пациентов с тяжелым COVID-19. Углубленный анализ около 200 иммунных параметров показал, что тяжесть заболевания, включая тяжелое воспаление и органную недостаточность, коррелирует с общей лимфопенией, при этом оставшиеся лимфоциты: CD4+ и CD8+ эффекторные Т-клетки, клетки TFH и короткоживущие плазматические клетки, продуцирующие антитела – высокоактивированы и потенциально гиперактивированы.
Вывод
Основные факторы, лежащие в основе различных реакций на SARS-CoV-2, остаются неясными. Одно из потенциальных направлений для будущих исследований – оценка того, может ли предшествующее инфицирование другими респираторными инфекциями или иммуноопосредованные состояния, такие как астма, повышать восприимчивость к коронавирусу SARS-CoV-2.
В большинстве исследований, посвященных оценке реакций приобретенного иммунитета к коронавирусу SARS-CoV-2, анализировались инфицированные взрослые. Такие исследования на детях носят более ограниченный характер. Понимание различий в приобретенных иммунных ответах между детьми и взрослыми – важная проблема в отношении SARS-CoV-2, потому что дети менее подвержены риску серьезных респираторных осложнений по сравнению со взрослыми, но у них может развиться опасный для жизни мультисистемный воспалительный синдром. Это может отражать измененное распознавание вируса иммунной системой у детей. Недавнее исследование, сравнивающее специфичность антител у взрослых и детей с инфекцией SARS-CoV-2, показало снижение разнообразия антител у детей и искаженный ответ на S-антитела IgG.
Исследования, оценивающие врожденный и приобретенный иммунный ответ, уточняющие взаимодействие между Т- и В-клетками и определяющие их связь с защитой от коронавируса, будут ключевыми для разработки стратегий, направленных на создание и усиление противовирусного иммунитета Т- и В-клеток.