Фолликулярная лимфома – злокачественная опухоль, которая образуется в лимфатических фолликулах из дефектных созревающих В-лимфоцитов. Около трети диагностированных случаев рака крови этого типа являются бессимптомными на поздней стадии заболевания.
Традиционное лечение фолликулярной лимфомы сочетает использование препарата моноклональных антител – ритуксимаба и противоопухолевой химиотерапии. Длительность основного лечения составляет 6 – 8 курсов, последующая поддерживающая терапия – еще 12 курсов. Примерно 80% пациентов достигают стойкой ремиссии, однако, почти у всех из них возникает рецидив. Поэтому есть клиническая потребность в новых методах лечения.
Коллектив врачей из Италии и Австралии исследовал методы стимуляции противоопухолевого иммунитета с помощью экспериментальной вакцины, которую вводили в опухоль. Ученые оценивали безопасность нового метода лечения и его клиническую эффективность.
Состав экспериментальной противоопухолевой вакцины
Главный компонент вакцины – дендритные клетки (ДК), обработанные интерфероном альфа-2b (ИФН-α2b) и колониестимулирующим белковым комплексом (GM-CSF), который ускоряет синтез лейкоцитов после химиотерапии. Для краткости такие дендритные клетки называют ИФН-ДК.
Дендритные клетки – критически важный элемент иммунной системы при вакцинации против рака. Во-первых, они находят и уничтожают раковые клетки. Во-вторых, дендритные клетки обучают другие клетки иммунной системы бороться с опухолью.
Воздействие интерферона-α2b на дендритные клетки значительно повышает их противоопухолевую эффективность. После такой обработки дендритные клетки:
- многократно увеличивают синтез противоопухолевых молекул;
- более эффективно обучают другие клетки иммунной системы распознавать раковые клетки;
- активнее поглощают клетки опухоли.
Иммунотерапия рака с помощью ИФН-ДК – прикладное и многообещающее направление терапии для стимуляции более широкого противоопухолевого иммунитета.
Второй компонент вакцины – ритуксимаб. Его доза существенно меньше, чем при традиционном лечении. Ритуксимаб – препарат мноклональных антител, сделанных методом генной инженерии. Эти антитела помогают иммунным клеткам находить клетки опухоли.
Доклинические исследования
До начала клинических исследований врачи изучили эффективность компонентного состава вакцины на культурах клеток и на мышах.
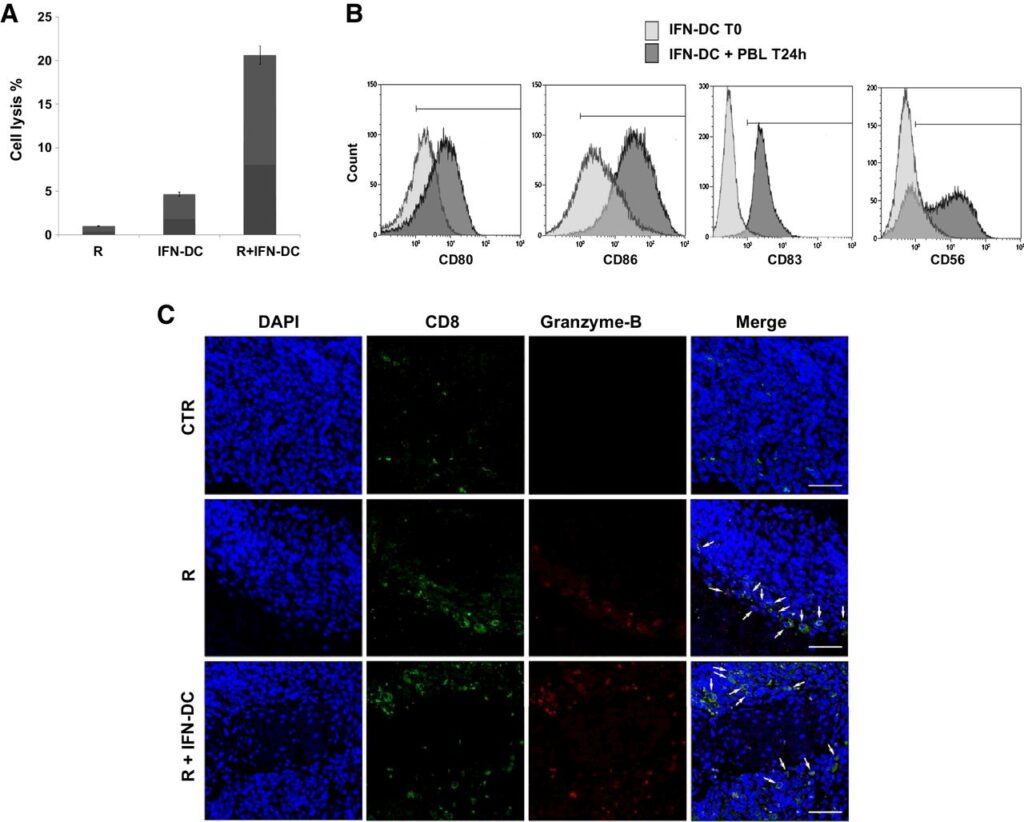
Сначала ученые сравнили эффективность ритуксимаба, ИФН-ДК, ИФН-ДК + ритуксимаб. В последнем случае соотношение ИФН-ДК и ритуксимаба было 5:1. В результате было установлено, что комбинированная терапия ИФН-ДК + ритуксимаб в 4 раза более эффективна для уничтожения клеток фолликулярной лимфомы, чем ИФН-ДК, и в 20 раз более эффективна, чем ритуксимаб (Рисунок А):
Источник изображения: https://aacrjournals.org/clincancerres/article/25/17/5231/81661/Clinical-and-Antitumor-Immune-Responses-in
Во втором доклиническом эксперименте ученые провели исследование на мышах, чтобы установить способность клеток ИФН-ДК закончить созревание при предварительной обработке ритуксимабом. Первоначально мышам вводили клетки фолликулярной лимфомы. После того как размер лимфомы достигал 4 мм, ученые вводили мышам 100 мкг ритуксимаба. Еще через сутки в опухоль вводили 2 миллиона клеток ИФН-ДК. Лечение повторяли каждые 7 дней, всего было сделано 3 инъекции. Через 14 дней ученые анализировали размер и состав опухоли.
Исследование на мышах показало, что предварительная обработка ритуксимабом способствовала тому, что в течение 24 часов ИФН-ДК закончили созревание и прошли стадию полной активации. Также ученые изучили, насколько сильно ИФН-ДК и ритуксимаб привлекают в опухоль другие иммунные клетки для уничтожения злокачественных клеток. В опухолях мышей, получавших ритуксимаб или ИФН-ДК + ритуксимаб, было больше CD8+ Т-лимфоцитов, чем у мышей в контрольной группе, не получавших лечение. Примечательно, что в группе мышей, получившей внутриопухолевую инъекцию ИФН-ДК, разрушение опухоли происходило изнутри (Рисунок С, на предыдущем изображении).
Ученые сделали вывод, что внутриопухолевый ИФН-ДК активирует противоопухолевый Т-клеточный иммунный ответ и увеличивает его силу.
Дизайн исследования, отбор пациентов, схема лечения
В исследовании участвовали 8 пациентов. У всех была подтвержденная биопсией фолликулярная лимфома, низкоопухолевая нагрузка, адекватное количество клеток крови, ожидаемая продолжительность жизни более 6 месяцев. В исследование не были включены пациенты с прогрессирующей лимфомой, нуждающиеся в стандартной терапии, ВИЧ-инфицированные, пациенты с аутоиммунными заболеваниями и беременные.
На первом этапе исследования врачи выращивали ИФН-ДК для каждого пациента. Сначала ученые производили забор периферической крови пациента. Потом из нее выделяли лейкоциты и моноциты. Когда содержание моноцитов достигало 60%, врачи начинали их культивирование в течение 3 дней в среде с интерфероном-α2b и колониестимулирующим белковым комплексом GM-CSF. Выращенные таким образом ИФН-ДК собирали, расфасовывали в дозы по 10 миллионов молекул и хранили в жидком азоте до момента использования.
Основная часть исследования проводилась с ноября 2014 по ноябрь 2017 года. Возраст пациентов был от 27 до 72 лет. У всех пациентов были увеличены лимфатические узлы или присутствовали поражения размером более 1.5 см в местах, доступных для местных инъекций и мониторинга лечения. Все инъекции делали в один пораженный поверхностный лимфоузел. Остальные пораженные лимфоузлы оставались без лечения для мониторинга результата.
В начале каждого цикла лечения пациентам водили низкую дозу ритуксимаба. Через 24 часа им вводили 10 миллионов клеток ИФН-ДК. Первые 4 цикла проводились каждые 2 недели, следующие 4 цикла – ежемесячно. Все процедуры проводились амбулаторно.
Результаты исследования
Безопасность лечения
Все пациенты хорошо переносили лечение. Только у одного пациента был небольшой отек и покраснение в месте инъекции. За 26 месяцев наблюдения ни у кого не развились аутоиммунные реакции.
Оценка клинического ответа
После окончания лечения у 4 участников исследования наблюдался клинический ответ. У 3 из них был полный клинический ответ. Ремиссия продолжается в 2 случаях, в течение 26 месяцев.
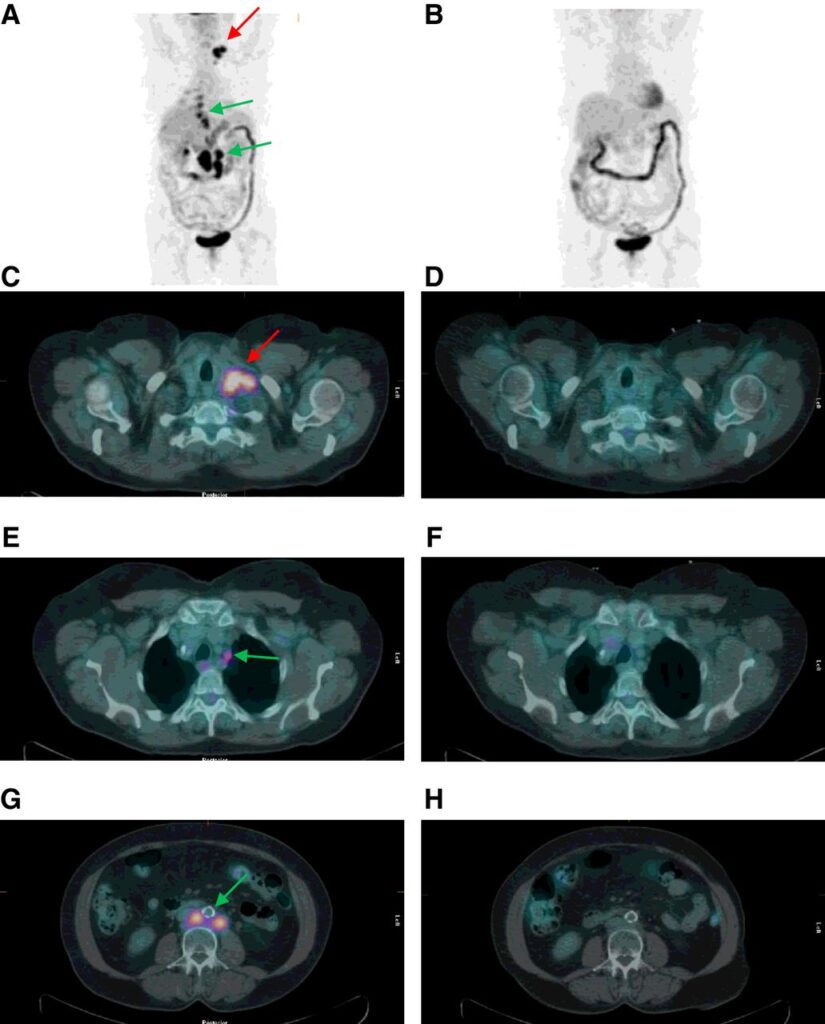
У одного пациента исчезла опухоль не только в лимфатическом узле, в который делались инъекции, но и в ряде других лимфоузлов, которые не подвергались лечению. Все поражения исчезли через 13 месяцев после начала лечения. Ремиссия продолжается уже 27 месяцев. Это указывает на проявление системного эффекта от лечения. Стрелками показаны пораженные участки до лечения, которые исчезли после лечения:
Источник изображения: https://aacrjournals.org/clincancerres/article/25/17/5231/81661/Clinical-and-Antitumor-Immune-Responses-in
Другой пациент подвергался интенсивному предварительному лечению до начала исследования. После начала лечения ритуксимабом и ИФН-ДК он достиг полного клинического ответа через 6 месяцев. Пациент умер через 22 месяца ремиссии в результате лечения острого миелоидного лейкоза.
Оценка противоопухолевых Т-клеточных ответов
В процессе лечения врачи оценивали биохимические показатели периферической крови пациентов. Было установлено, что более высокие уровни опухолеспецифических Т-клеточных ответов наблюдались у пациентов с клиническим ответом на лечение. У пациента, клинически не отвечающего на терапию, была едва заметная индукция Т-клеточного ответа.
Ученые делают вывод, что лечение ритуксимабом и ИФН-ДК вызывает системные противоопухолевые Т-клеточные ответы.
Выводы
Исследование продемонстрировало, что комбинированная терапия ИФН-ДК и низкими дозами ритуксимаба безопасна и клинически обоснована для пациентов с фолликулярной лимфомой, прошедших интенсивное лечение. ИФН-ДК эффективен в индукции клинического ответа и в стимуляции выработки опухолеспецифических Т-клеток.
Ученые подчеркивают, что в их схеме лечения отсутствовала лучевая терапия, и одного ритуксимаба достаточно для стимулирования опухолевых антигенов.
Исследование проведено на небольшой выборке пациентов. Поэтому для подтверждения эффективности метода нужны большие когортные исследования.
Полезная статья, нужная информация? Поделитесь ею!
Кому-то она тоже будет полезной и нужной: