Бактерия Хеликобактер пилори заразила более половины населения мира. Эта бактерия является основной причиной гастрита, язвы, рака желудка. Ученые до сих пор исследуют механизмы, которые позволяют Хеликобактер защищаться от иммунной системы и вызывать хроническую инфекцию.
Один из механизмов открыла в 2013 году международная группа ученых из Университета Копенгагена (Дания) и Университета Монаша (Австралия). Ученые установили, что бактерия выделяет токсин VacA, который блокирует выработку интерферона-бета (ИФН-β), стимулируемую пробиотиками. Так Хеликобактер препятствует запуску адаптивного иммунитета.
Предпосылки исследования
Более ранние исследования, проведенные в 2010-2012 годах этой же группой ученых, показали, что пробиотическая бактерия Lactobacillus acidophilus стимулирует выработку ИФН-β иммунными клетками. Более того, L.acidophilus оказалась самым эффективным стимулятором среди всех исследованных 46 штаммов пробиотиков.
Еще более ранние клинические и лабораторные исследования, проведенные в 2006-2007 годах в Швейцарии, Италии и Японии, показали, что употребление пробиотиков уменьшает численность Хеликобактер пилори и снижает побочные эффекты при стандартном лечении антибиотиками.
Однако есть и другое исследование 2011 года, проведенное португальскими учеными на пациентах с язвенной болезнью и язвенными рубцами. Это исследование не показало пользу от L.acidophilus при лечении Хеликобактер одновременно двумя антибиотиками.
Таким образом, в одних случаях пробиотики стимулируют выработку интерферона-бета и запуск адаптивного иммунитета против Хеликобактер пилори, а в других этого почему-то не происходит. Цель данного исследования ученые сформулировали так:
- установить причину отсутствия синтеза ИФН-β;
- определить условия, в которых выработка интерферона-бета все-таки возможна.
Дизайн исследования
Для экспериментов ученые использовали макрофаги — основной тип иммунных клеток, который уничтожает Хеликобактер пилори. Второй участник эксперимента – пробиотическая бактерия L.acidophilus, которая наиболее эффективно стимулирует выработку макрофагами интерферона-бета с последующим запуском адаптивного иммунитета.
Были использованы два типа бактерий Хеликобактер:
- дикого типа — для моделирования среды, максимально приближенной к естественной;
- генно-модифицированные бактерии — для детального изучения особенностей взаимодействия пробиотической бактерии и Хеликобактер пилори.
Макрофагов последовательно стимулировали сначала только L.acidophilus, потом только Хеликобактер. А в заключении — обоими типами бактерий одновременно. Ученые стремились выявить различия в иммунных реакциях.
Результаты
Уровни синтеза интерферона-бета
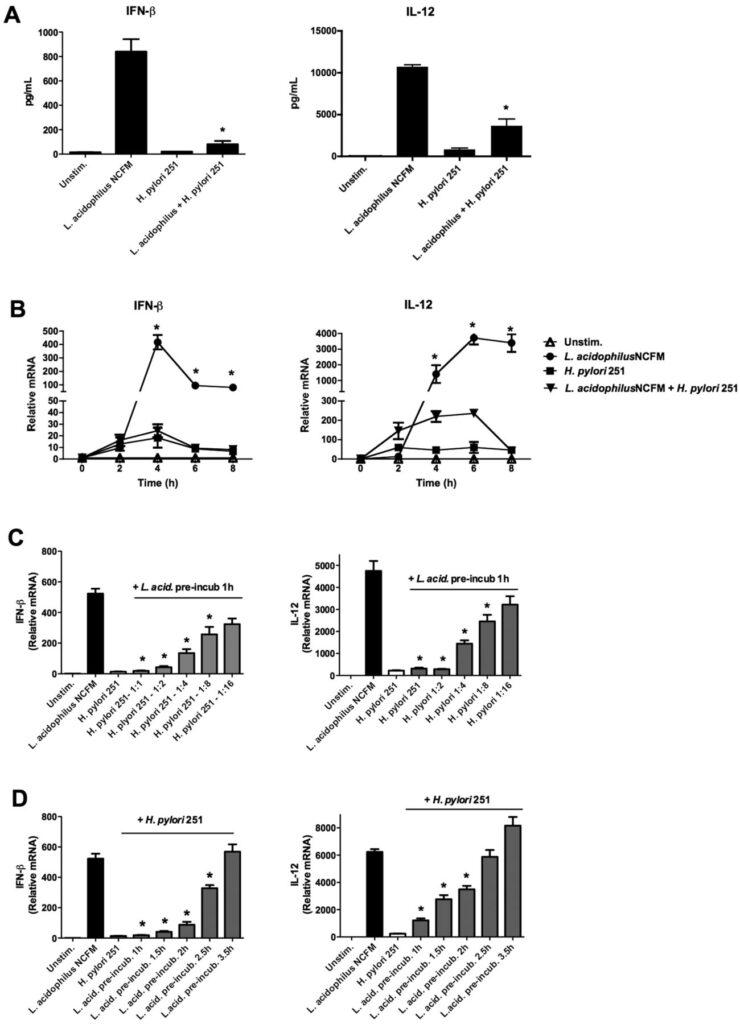
Сначала ученые убедились, что L.acidophilus способны запускать выработку интерферона-бета макрофагами. Оказалось, что через 10 часов после добавления пробиотика к макрофагам уровень ИФН-β значительно возрастает до 840 пг/мл. Также значительно возрастает до 10 700 пг/мл уровень другого сигнального белка — IL-12, который способствует созреванию иммунных клеток и запускает выработку белков иммунной защиты.
При стимуляции макрофагов только Хеликобактер уровни выработки ИФН-β и IL-12 были ощутимо ниже — 20 пг/мл и 850 пг/мл соответственно.
В следующем эксперименте ученые наблюдали комбинированное воздействие разного типа бактерий на макрофаги. Сначала ученые в течение одного часа обрабатывали макрофаги пробиотиком, а затем добавили Хеликобактер пилори дикого типа. В результате после добавления Хеликобактер общая выработка интерферона-бета снизилась на 90%, а IL-12 – на 66%.
Полученные результаты представлены на рисунке ниже (графики А).
Динамика выработки интерферона-бета
Чтобы определить динамику синтеза интерферона, ученые делали замеры через 2, 4, 6 и 8 часов после начала эксперимента. Максимум выработки интерферона-бета достигался через 4 часа. Причем при стимуляции макрофагов только L.acidophilus объем синтеза возрастал в 400 раз по сравнению с контрольной группой. При стимуляции только Хеликобактер пилори — возрастал в 15 раз.
Когда к макрофагам после стимуляции пробиотиком добавляли Хеликобактер, выработка ИФН-β полностью блокировалась, а синтез IL-12 снижался на 94%.
Полученные результаты представлены на рисунке ниже (графики В).
При каком соотношении Хеликобактер пилори к пробиотику восстанавливается синтез интерферона
Все предыдущие эксперименты проводились, когда концентрации Хеликобактер пилори и L.acidophilus были одинаковыми (1:1). Поэтому ученые решили установить, при каком соотношении пробиотика к Хеликобактеру восстанавливается синтез интерферона-бета. Эксперименты проводились для случаев, когда концентрация пробиотика была в 2, 4, 8 и 16 раз выше, чем Хеликобактер пилори.
Даже при концентрации 1:8 синтез интерферона-бета был ниже на 51%. И только при концентрации 1:16 влияние Хеликобактера становилось незначительным.
Полученные результаты представлены на рисунке ниже (графики С).
Ученые предположили, что причина – не в отрицательном влиянии отдельно взятой бактерии, а в веществах, которые Хеликобактер вырабатывает для подавления иммунной системы.
Сколько нужно стимулировать макрофаги пробиотиком, чтобы уменьшить негативное влияние Хеликобактер пилори
Через 1,5 часа стимуляции пробиотиком и после следующего за стимуляцией добавления Хеликобактер выработка ИФН-β снижалась на 92%. Через 2 часа — снижалась на 83%, через 2,5 часа — на 63%. Отрицательное влияние на синтез ИФН-β полностью прекращалось через 3,5 часа.
Полученные результаты представлены на рисунке ниже (графики D).
Рисунок:
Источник изображения: https://journals.asm.org/doi/full/10.1128/mBio.00609-12
Генетический анализ макрофагов, стимулированных Хеликобактер пилори или L.acidophilus
Чтобы оценить масштаб влияния Хеликобактер, ученые подсчитали количество генов макрофагов, активируемых или подавленных в случае:
- стимуляции только L.acidophilus;
- стимуляции только Хеликобактер пилори;
- совместной стимуляции Хеликобактер пилори и L.acidophilus в концентрации 1:1.
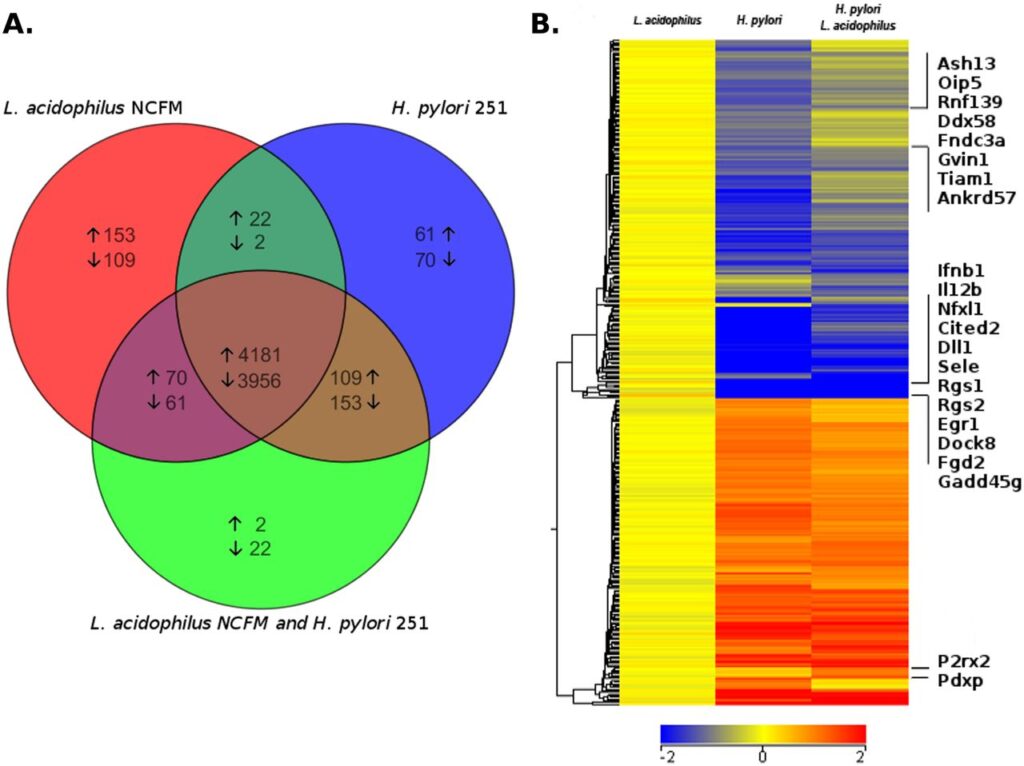
Во всех случаях повышалась активность 4 181 гена, понижалась — 3 956 генов. При стимуляции L.acidophilus повышалась активность генов, отвечающих за адаптивный иммунитет. В частности, стимулировались гены врожденного иммунитета, способствующие развитию адаптивного иммунитета, среди которых – гены, связанные с синтезом интерферона-бета.
При стимуляции бактерией Хеликобактер активировались гены, отвечающие только за врожденный иммунитет, а гены адаптивного иммунитета были подавлены:
Источник изображения: https://journals.asm.org/doi/full/10.1128/mBio.00609-12
Найден токсин, который помогает Хеликобактер подавлять синтез ИФН-β
В 2000 году ученые из Университета Бирмингема (Великобритания) исследовали влияние токсина VacA, вырабатываемого Хеликобактер, на эпителиальные клетки. Токсин VacA способствовал образованию в клетках кислых вакуолей и нарушению структуры клеточной мембраны, что ухудшало защитные свойства слизи, выстилающей желудок.
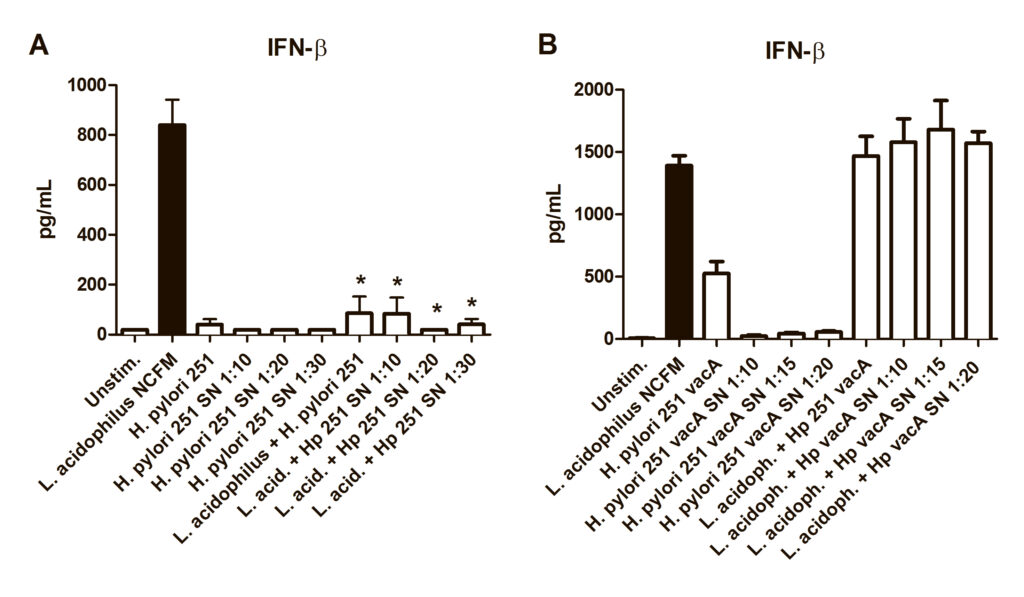
В настоящем исследовании ученые предположили, что этот же токсин VacA может подавлять выработку ИФН-β в макрофагах. Для проверки гипотезы ученые использовали генно-модифицированный штамм Хеликобактер, не способный вырабатывать нужный токсин. Генно-модифицированный штамм не влияет на синтез интерферона-бета, в отличие от Хеликобактер дикого типа:
Источник изображения: https://journals.asm.org/doi/full/10.1128/mBio.00609-12
Выводы
Пробиотики снижают численность Хеликобактер пилори. Эффект основан на стимуляции выработки белков, запускающих адаптивный иммунитет, в частности – интерферона-бета.
Однако Хеликобактер способна подавлять положительное влияние пробиотиков и блокировать синтез ИФН-β. Отрицательный эффект нивелируется, кода численность пробиотических бактерий в 16 раз превышает численность Хеликобактер. Выработка интерферона также не блокируется, если иммунные клетки предварительно обработать пробиотиком в течение 3,5 часов.
Механизм, с помощью которого Хеликобактер нарушает синтез ИФН-β, основан на выработке токсина VacA. Этот токсин образует в иммунных клетках кислые вакуоли и нарушает структуру клеточных мембран. Генно-модифицированный штамм Хеликобактер, который лишен способности синтезировать токсин VacA, не способен блокировать выработку интерферона-бета.
Полезная статья, нужная информация? Поделитесь ею!
Кому-то она тоже будет полезной и нужной:
Источники
- Helicobacter pylori VacA Suppresses Lactobacillus acidophilus-Induced Interferon Beta Signaling in Macrophages via Alterations in the Endocytic Pathway
- MyD88 Drives the IFN-β Response to Lactobacillus acidophilus in Dendritic Cells through a Mechanism Involving IRF1, IRF3, and IRF7
- Helicobacter pylori and Probiotics
- Lactobacillus reuteri therapy to reduce side-effects during anti-Helicobacter pylori treatment in children: a randomized placebo controlled trial
- Effect of Bifidobacterium bifidum Fermented Milk on Helicobacter pylori and Serum Pepsinogen Levels in Humans
- Lactobacilli and bifidobacteria induce differential interferon-β profiles in dendritic cells
- Evaluation of Helicobacter pylori eradication by triple therapy plus Lactobacillus acidophilus compared to triple therapy alone
- Interleukin-12 and the regulation of innate resistance and adaptive immunity
- Cell Vacuolation Induced by the VacA Cytotoxin of Helicobacter pylori Is Regulated by the Rac1 GTPase